
I RAGGI-X
LA GRANDEZZA INCOGNITA
Così Wilhelm Conrad Röntgen commentò l’origine del nome della sua strepitosa scoperta."Non avevo idea di cosa fossero quei raggi perciò li chiamai semplicemente raggi X, essendo x il simbolo matematico di una grandezza incognita".
LA NATURA DEI RAGGI-X
I raggi X sono radiazioni elettromagnetiche ionizzanti con lunghezze d'onda comprese approssimativamente tra 10 nm e 0,01 nm. Sono divisi in raggi X molli, con lunghezze d'onda superiori a 0,1 nm, e raggi X duri, con lunghezze d'onda inferiori a questa soglia.Grazie alla loro lunghezza d'onda ridotta e all'energia associata, i raggi X trovano ampio utilizzo in campo medico, industriale e nei beni culturali.Consentono di analizzare internamente corpi e oggetti in modo non distruttivo.

Spettro elettromagnetico
LA PRODUZIONE DI RAGGI-X
Ogni volta che un elettrone di un atomo subisce una transizione da un livello energetico a un altro, si verifica l'emissione di raggi X monocromatici.Queste transizioni avvengono, ad esempio, quando gli elettroni subiscono un processo a cascata in un tubo a raggi X.I raggi X hanno un'energia sufficiente per liberare gli elettroni più interni degli atomi, causando la ricaduta degli elettroni più esterni nei livelli energetici lasciati vuoti.Queste transizioni sono accompagnate dall'emissione di radiazione X. La lunghezza d'onda dei raggi X emessi dipende dal salto di energia compiuto dagli elettroni durante la transizione e dalla struttura orbitale degli atomi coinvolti.L'analisi della radiazione X caratteristica emessa da un campione di materiale sconosciuto consente di determinare la sua composizione.Lo spettro energetico dei raggi X è costituito da due componenti principali: la radiazione continua di frenamento (bremssstrahlung) e la radiazione caratteristica.

RADIAZIONE DI BREMSSTRAHLUNG
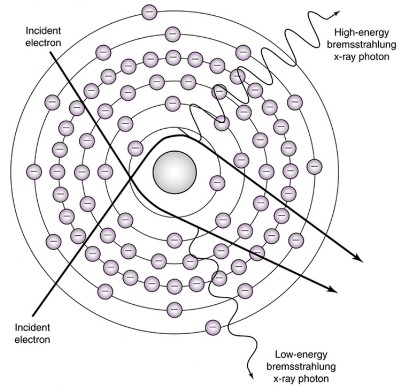
La radiazione continua di frenamento, conosciuta anche come radiazione di bremsstrahlung, è la radiazione emessa da particelle cariche libere quando subiscono accelerazione o decelerazione a causa dell'interazione con il campo elettrico di un nucleo atomico.L'intensità di questa radiazione è inversamente proporzionale al cubo della massa della particella interagente.Lo spettro generato dalla radiazione di frenamento varia in modo continuo (insieme alla frequenza) da 0 a un valore massimo pari all'energia cinetica degli elettroni che interagiscono, ed è quindi di tipo continuo.
EFFETTO COMPTON
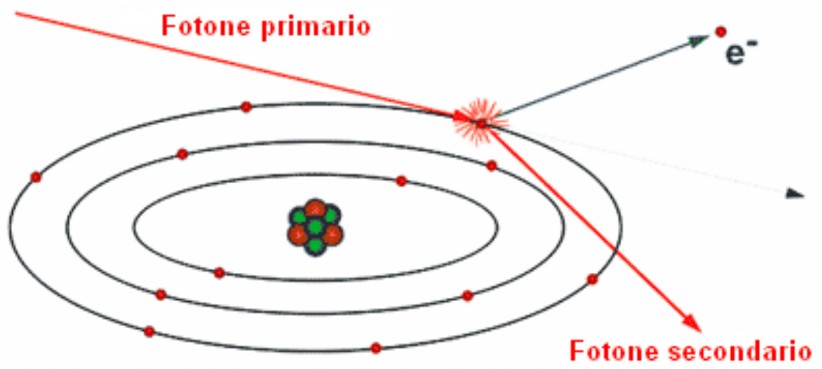
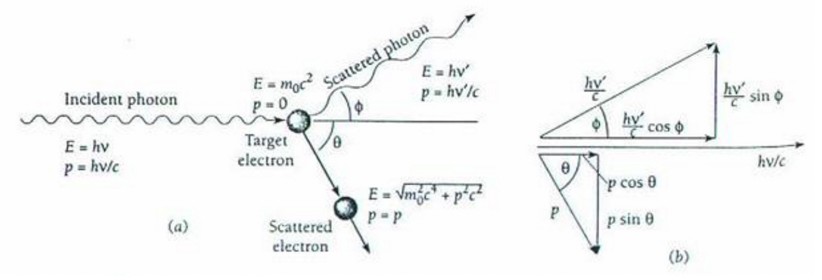
Secondo la teoria quantistica, i fotoni si comportano come particelle, ad eccezione della loro mancanza di massa a riposo.Nel 1922, Arthur Compton analizzò lo spettro delle onde elettromagnetiche, in particolare dei raggi X, e osservò due righe spettrali distinte nel processo di scattering.Una riga riproduceva fedelmente la frequenza della radiazione incidente ed era in accordo con la teoria classica, mentre l'altra aveva una frequenza minore (lunghezza d'onda maggiore) che poteva essere spiegata solo con la teoria quantistica.Secondo la teoria classica dell'elettromagnetismo, gli elettroni "bersaglio", una volta eccitati dai fotoni incidenti, oscillano alla stessa frequenza della radiazione incidente, emettendo radiazione della stessa frequenza, indipendentemente dalla direzione di diffusione.Tuttavia, secondo la teoria quantistica, avviene un fenomeno di urto tra fotoni ed elettroni periferici, in cui gli elettroni assorbono parte dell'energia dei fotoni, risultando in una frequenza minore dipendente dall'angolo di scattering.Quando un fotone X colpisce un elettrone e viene diffuso dalla sua direzione iniziale, l'elettrone riceve un impulso e inizia a muoversi.Si può considerare che l'energia persa dal fotone nella collisione viene guadagnata dall'elettrone sotto forma di energia cinetica, anche se sono coinvolti diversi fotoni.
RADIAZIONE CARATTERISTICA
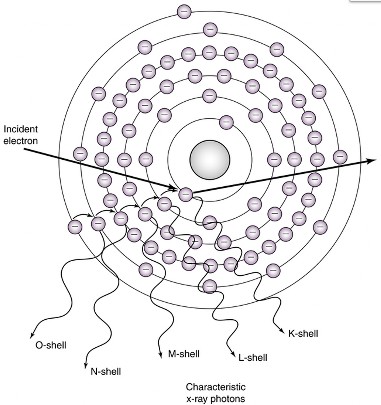
La radiazione caratteristica rappresenta la parte discreta dello spettro energetico dei raggi X.Quando un elettrone incidente collide con uno degli elettroni più interni di un atomo, crea una lacuna nella sua orbita, che viene successivamente riempita da uno degli elettroni più esterni.Questo processo è responsabile della produzione di raggi X, e l'energia corrispondente dipende dal tipo di materiale bersaglio, chiamato anche target.Pertanto, questa radiazione viene definita "caratteristica".
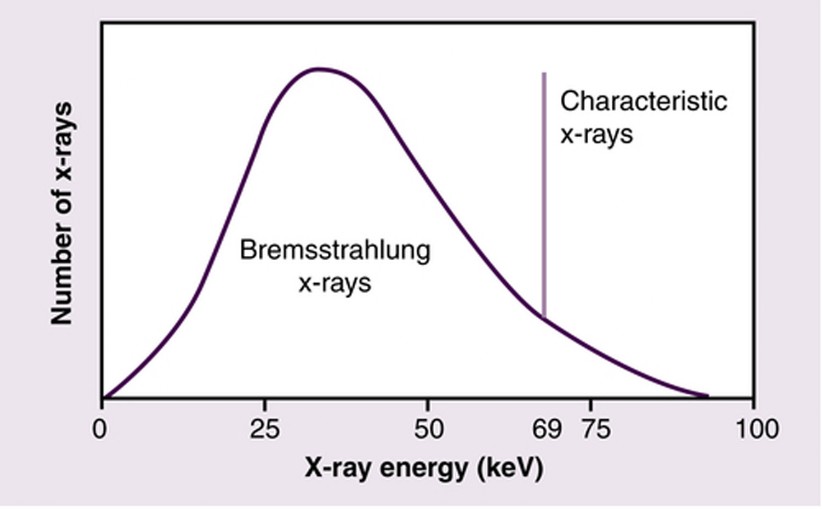
Spettro caratteristico
I raggi X svolgono un ruolo fondamentale e di grande importanza nell'industria.Nel settore metallurgico, vengono utilizzati nelle tecniche di controllo non distruttivo (CND) per la verifica della qualità delle leghe metalliche ottenute per fusione e per la verifica interna di componenti.Le immagini a raggi X consentono di individuare eventuali irregolarità o difetti nei componenti.Tecniche simili vengono applicate per valutare l'autenticità di altri prodotti industriali, pietre preziose e opere d'arte.
IONIZZAZIONE
Il processo di ionizzazione si riferisce al fenomeno in cui un atomo o una molecola può perdere o guadagnare elettroni, creando particelle chiamate ioni.Gli ioni sono carichi elettricamente, e la loro carica dipende dal numero di elettroni persi o acquisiti durante il processo di ionizzazione.
ISOTOPI
Nella natura sono noti più di 100 elementi, ognuno dei quali è caratterizzato dal suo numero atomico Z (il numero di protoni nel nucleo o il numero di elettroni che circondano il nucleo).La struttura di un atomo richiede una correlazione tra il numero atomico (Z) e il numero di massa (A) (il numero totale di protoni e neutroni nel nucleo).Si è scoperto che esistono elementi con lo stesso numero atomico (Z) ma con diversi numeri di massa (A), e questi vengono chiamati isotopi.Gli isotopi di un determinato elemento hanno lo stesso numero di protoni ma differiscono per il numero di neutroni nel nucleo.Alcuni isotopi possono essere instabili, cioè hanno un eccesso di energia che viene rilasciato sotto forma diradiazione elettromagnetica, in un processo chiamato radioattività.


 Italiano
Italiano English
English Español
Español Français
Français Deutsch
Deutsch العربية
العربية